Цервидил (динопростон 10 мг, система вагинальная терапевтическая)
Предназначен для стимуляции созревания шейки матки при доношенном сроке беременности
(от 37 полных недель гестации) для использования в течение 24-часового периода.
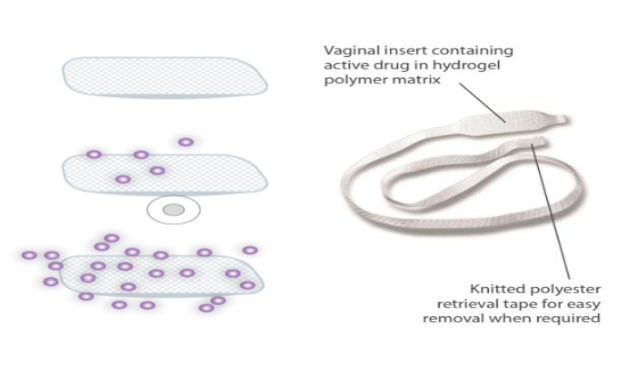
- Вагинальная система, содержит активное лекарственное средство динопростон в количестве 10 мг, которое распределено в полимерной гидрогелиевой матрице
- Система обеспечивает контролируемое высвобождение препарата по 0,3 мг/час в области шейки матки в течение 24 часов
- Система содержит длинную ленту, что позволяет при необходимости немедленно извлечь вкладку
- Систему следует извлечь через 24 ч независимо от степени созревания шейки матки
- Препарат не требует размораживания перед использованием, вводится в верхнюю часть заднего свода влагалища с возможным использованием гидрогеля (смазки)
- Окситоцин рекомендуется вводить не ранее чем через 30 минут после извлечения вкладыша
- Препарат хранится в морозильной камере при температуре -25-10 С, не подлежит повторному замораживанию
1. Инструкция применения препарата Цервидил для врача
Инструкция содержит всю необходимую информацию по препарату. Приведена краткая характеристика препарата Цервидил (качественный и количественный состав, форма выпуска, показания, режим дозирования; способ применения содержит информацию по введению, а также рекомендации по извлечению препарата и по каким причинам необходимо это делать).
В разделе показания к применению указано, что препарат предназначен для стимуляции созревания шейки матки у беременных в возрасте от 18 лет и старше при сроке гестации ≥ 37 недель, при наличии медицинских или акушерских показаний для индукции родовой деятельности.
В инструкции содержится раздел по противопоказаниям и особым указаниям и мерам предосторожности, указано взаимодействие с другими лекарственными препаратами, а также нежелательные явления.
Раздел фармакологические свойства содержит механизм действия, фармакодинамические эффекты, абсорбцию и распределение, биотрансформацию и элиминацию, а также данные по доклинической безопасности.
Раздел срок годности и особые меры предосторожности при хранении содержит информацию о хранении препарата в морозильной камере при температуре от -25 °С до -10 °С в оригинальной упаковке (саше в пачке картонной).
2. Листок- вкладыш информация для пациента
Листок-вкладыш -информация для пациента содержит информацию по препарату Цервидил, 10 мг, система вагинальная терапевтическая с действующим веществом динопростон.
Листок-вкладыш по препарату содержит 6 основных разделов.
- Что из себя представляет препарат Цервидил, и для чего его применяют.
- О чем следует знать перед применением препарата Цервидил.
- Применение препарата Цервидил.
- Возможные нежелательные реакции.
- Возможные нежелательные реакции.
- Содержимое упаковки и прочие сведения
3. Цервидил – пособие по применению для врача
Содержит информацию по технике введения препарата Цервидил, как правильно расположить систему между между средним и указательным пальцами, чтобы конец пластины, который будет введён, первым был направлен вперед; информацию по технике извлечения, данные по безопасности, особые указания, меры предосторожности и практические советы для врача.
4. Установка системы СВТ (система вагинальная терапевтическая)
На слайде 5 и 6 приведены этапы установки системы вагинальной терапевтической от момента вскрытия упаковки до установки СВТ системы.
5. Цервидил – характеристика препарата
Приведена краткая информация по препарату и описание СВТ системы, общие характеристики препарата, режим дозирования, противопоказания и меры предосторожности.
6. Цервидил – данные по эффективности
Информация для каких пациентов показан препарат, скорость высвобождения действующего вещества, общие характеристики препарата, особенности хранения, данные по эффективности в монопротоколе в сравнении с разными опциями (плацебо, Пропедил гель, Катетер Фолея), а также данные по эффективности в комбинированном протоколе в сравнении с катетером Фолея. Приведены данные по переносимости и безопасности.
7. Статья Narayanan Vallikkannu et all, 2021 год - приведено сравнение эффективности комбинированного режима использования Цервидила и катетер Фолея vs катетер Фолея
Narayanan Vallikkannu , Naumi Laboh , Peng Chiong Tan, Jesrine Gek Shan Hong, Mukhri Hamdan, Boon Kiong Lim, 2021 г., Archives of Gynecology and Obstetrics (2022) 306:1027–1036 https://doi.org/10.1007/s00404-021-06383-2
«Использование катетера Фолея и динопростона с контролируемым высвобождением по сравнению с использованием только катетера Фолея для индукции родовой деятельности у первородящих женщин: рандомизированное исследование»
Рандомизированное исследование было проведено в университетской клинике в Малайзии в период с декабря 2018 г. по май 2019 г. Первородящие женщины с доношенной беременностью и неудовлетворительным состоянием шейки матки (оценка по шкале Бишопа ≤ 5 баллов), у которых было запланировано проведение индукции родовой деятельности, были рандомизированы в группу использования катетера Фолея с одновременным введением динопростона с контролируемым высвобождением или в группу использования только катетера Фолея.
В исследование у первородящих женщин время до вагинальных родов составило 22,5 часа в группе комбинированной терапии Цервидил+ катетер Фолея, а в группе использования только катетер Фолеявремя составило 35,3 часа (р<0,001). Комбинированная терапия сокращает время до начала родов на 12,6 ч.
Основной вывод статьи: у первородящих женщин с незрелой шейкой матки при доношенной беременности комбинированное использование катетера Фолея и вагинального вкладыша с динопростоном с контролируемым высвобождением, по сравнению с использованием только катетера Фолея, способствовало сокращению продолжительности индукции родовой деятельности до вагинального родоразрешения и частоты кесарева сечения.
8. Статья Ahmet Eser at all, 2019 год - приведено сравнение эффективности монорежима Цервидила и комбинированного режима использования Цервидила с катетер Фолея
Ahmet Eser · Enis Ozkaya, Cigdem Yayla Abide, Tugba Eser, Gulcin Yildirim Eser, Faruk Abike, Ahter Tanay Tayyar, Mustafa Eroglu., Archives of Gynecology and Obstetrics (2019) 299:451–457 https://doi.org/10.1007/s00404-018-4998-8
Трансцервикальное введение баллонного катетера Фолея в комбинации с вагинальным вкладышем с простагландином E2 по сравнению с использованием только вагинального вкладыша с простагландином E2 для индукции родовой деятельности при доношенной беременности: рандомизированное клиническое исследование.
В исследование были включены пациентки с незрелой шейкой матки, которым требовалась индукция родовой деятельности. В общей сложности этом проспективном рандомизированном исследовании были проанализированы данные 294 женщин: в группе 1 (контрольная группа): индукция родовой деятельности только с интравагинальным введением вагинального вкладыша с PgE2 (n = 148), и группа 2 (исследуемая группа): интрацервикальное введение баллонного катетера Фолея в дополнение к интравагинальному введению вкладыша с PgE2 (n = 146). Первичный исходом в этом исследовании был период от начала индукции до родоразрешения. Вторичным исходом был период от начала индукции до активной фазы родов.
При анализе данных первородящих беременных женщин было показано, что комбинация интрацервикального введения баллонного катетера Фолея с интравагинальным введением вкладыша с PgE2 было связано с сокращением времени от начала индукции до развития активной фазы родов (1000 мин по сравнению с 585 мин, P < 0,001) и до родоразрешения (1386 мин по сравнению с 1001 мин, P < 0,001). ). Комбинированная терапия сокращает время до начала родов в среднем на7 часов и сокращает на 6,4 часа до родоразрешения.
9. Статья Rodney K. Edwards at all, 2019 - приведено сравнение эффективности комбинированного режима использования Цервидила и катетер Фолея vs катетер Фолея
Rodney K. Edwards, Michelle L. Norris1, Mitchell D. West2, Christina Zornes1, Katherine A. Loeffler1, Jennifer D. Peck, 2009 г., American Journal of Obstetrics & Gynecology
Применение динопростона с контролируемым высвобождением и катетер Фолея по сравнению с использованием только катетер Фолея: рандомизированное контролируемое исследование.
Пациентки с неповрежденными плодными оболочками, с неблагоприятными параметрами шейки матки (расширение ≤ 2 см; если 2 см, то сглаживание < 80 %), сроком беременности ≥ 37 недель были рандомизированы в группу СВТ + катетер Фолея или в группу катетера Фолея со стратификацией по количеству родов в анамнезе (первородящие или повторнородящие), n=100.
В представленных результатах исследования у первородящих женщин время до вагинальных родов составило 21,2 часа в группе комбинированной терапии Цервидил+ катетер Фолея, а в группе использования только катетер Фолея время составило 31,3 часа (р=0,052).
Основной вывод статьи: по сравнению с использованием только катетера Фолея комбинированное использование катетера Фолея с вагинальным вкладышем с динопростоном для созревания шейки матки и индукции родовой деятельности способствовало сокращению времени до вагинального родоразрешения у первородящих женщин на 10 часов.

